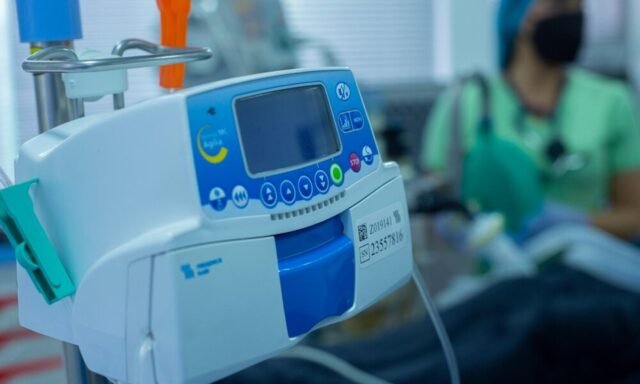
La fabricación de dispositivos médicos no se trata sólo de producir piezas que cumplan con las especificaciones. Se trata de ofrecer constantemente productos seguros y confiables en un entorno donde la variabilidad puede tener consecuencias graves. Una pequeña desviación en un producto de consumo puede resultar en inconvenientes. En un dispositivo médico, podría provocar daños al paciente.
Entonces, ¿qué define una estrategia de producción sólida en este contexto? ¿Es velocidad, automatización, control de costos o cumplimiento normativo? En realidad, es la capacidad de equilibrar todo esto manteniendo una calidad constante en condiciones variables. Este equilibrio no se produce por casualidad. Se construye deliberadamente, proceso a proceso.
Alinear la fabricación con las expectativas regulatorias
Una estrategia de producción en el sector de dispositivos médicos no puede existir independientemente de los requisitos reglamentarios. Marcos como ISO 13485, el MDR de la UE y el Reglamento del sistema de calidad de la FDA esperan que los fabricantes demuestren control, trazabilidad y pensamiento basado en riesgos.
¿Por qué es esto importante a nivel estratégico? Porque el cumplimiento no se consigue reaccionando a las auditorías. Esto se logra incorporando el pensamiento regulatorio en las decisiones de fabricación cotidianas.
Por ejemplo, al seleccionar un proveedor, la pregunta no debería ser sólo si puede cumplir con las expectativas de costos y volumen. También debería ser si pueden demostrar control de procesos, disciplina de documentación y prácticas de gestión de cambios alineadas con las regulaciones de dispositivos médicos. Una estrategia sólida anticipa el escrutinio regulatorio mucho antes de que ocurra.
Control de Procesos como Base
La solidez de la fabricación comienza con el control del proceso. Cada etapa de producción debe ser comprendida, documentada y monitoreada. Pero ¿qué significa realmente “entendido”?
Significa saber qué parámetros son críticos, qué tolerancias afectan la seguridad y qué variaciones pueden aceptarse sin comprometer el rendimiento. Sin esta claridad, los fabricantes actúan de forma reactiva, solucionando los problemas cuando aparecen en lugar de prevenirlos.
Considere un proceso de sellado para envases estériles. Si las variaciones de temperatura y presión no se controlan estrictamente, la esterilidad puede verse comprometida. El dispositivo en sí puede ser perfecto, pero un defecto en el embalaje podría hacerlo inseguro. Estrategias sólidas identifican estos procesos críticos de manera temprana y aplican mecanismos de control apropiados.
Cuando la verificación no es suficiente
No todos los resultados de fabricación se pueden verificar completamente sin dañar el producto. Esta realidad introduce uno de los pilares más importantes de la estrategia productiva: la validación.
Si un proceso produce resultados que no pueden confirmarse únicamente mediante inspecciones de rutina, ¿cómo puede un fabricante demostrar coherencia? La respuesta está en actividades de validación estructuradas que proporcionen evidencia de que el proceso produce resultados conformes de manera confiable.
Cuando la verificación por sí sola no puede proporcionar suficiente seguridad, los fabricantes confían validación de procesos de dispositivos médicos demostrar que las condiciones de producción producen consistentemente productos seguros y conformes. Esto no es sólo una formalidad regulatoria. Es una salvaguardia contra defectos que de otro modo podrían permanecer ocultos hasta que los productos lleguen a los pacientes.
De esta forma, la validación pasa a formar parte del control estratégico de riesgos y no a una tarea técnica aislada.
Gestionar el cambio sin perder el control
Los entornos de fabricación rara vez permanecen estáticos. El equipo está actualizado. Se reubican las líneas de producción. Se reemplazan proveedores. Cada cambio introduce una variabilidad potencial.
Una estrategia sólida no puede resistir el cambio. Él lo maneja. Antes de implementar modificaciones, los fabricantes deben evaluar el impacto potencial en la seguridad, el rendimiento y el cumplimiento normativo. Incluso ajustes aparentemente pequeños, como cambiar la configuración de una máquina o reemplazar materias primas, pueden alterar las características del producto.
¿Por qué los reguladores ponen tanto énfasis en el control de cambios? Porque la historia muestra que muchas no conformidades surgen no de fallas de diseño iniciales, sino de cambios mal administrados. Una estrategia de producción madura trata el cambio como un proceso estructurado y no como un atajo operativo.
Supervisión y subcontratación de proveedores.
Pocos fabricantes de dispositivos médicos operan íntegramente internamente. La subcontratación y las cadenas de suministro globales son comunes. Pero la delegación no elimina la responsabilidad.
Si un componente crítico se produce externamente, ¿cómo garantiza un fabricante su calidad constante? A través de la calificación de proveedores, auditorías periódicas, seguimiento del desempeño y claridad contractual.
Una estrategia sólida reconoce que el desempeño del proveedor impacta directamente en la seguridad del paciente. Establece expectativas por adelantado y verifica su cumplimiento periódicamente. Sin esta supervisión, la variabilidad puede entrar al sistema sin ser detectada hasta convertirse en una cuestión regulatoria.
Capacitación y factores humanos en la manufactura
Los procesos y la documentación son tan confiables como las personas que los implementan. La capacitación a menudo se considera administrativa, pero desempeña un papel central en el mantenimiento de la integridad de la producción.
¿Están los operadores conscientes de los parámetros críticos? ¿Entienden el impacto de las desviaciones? ¿Pueden reconocer las primeras señales de alerta de una desviación del proceso?
Una estrategia que descuida la competencia humana corre el riesgo de socavar incluso el sistema más cuidadosamente diseñado. La capacitación continua y una rendición de cuentas clara garantizan que los procedimientos se traduzcan en una ejecución coherente.
Mejora continua basada en datos
Una estrategia de producción sólida no aspira a la perfección en el lanzamiento; aspira a una mejora controlada a lo largo del tiempo. Los datos de quejas, no conformidades y métricas de producción brindan información sobre las tendencias de desempeño.
Si las tasas de defectos aumentan gradualmente, ¿la organización lo detectará tan temprano? Si la capacidad del proceso comienza a disminuir, ¿existe algún mecanismo de intervención? El monitoreo continuo convierte los datos sin procesar en retroalimentación estratégica.
Este enfoque proactivo reduce el riesgo de retirada, mejora la eficiencia y fortalece la confianza regulatoria.
Conclusión
Construir una estrategia de fabricación sólida para dispositivos médicos requiere más que eficiencia operativa. Requiere un control de procesos estructurado, una gestión disciplinada del cambio, supervisión y validación de proveedores cuando la verificación por sí sola es insuficiente.
El objetivo no es simplemente pasar auditorías, sino garantizar que cada dispositivo que sale de la línea de producción funcione como se espera en condiciones del mundo real. Cuando la estrategia integra el cumplimiento, la gestión de riesgos y la mejora continua, la producción se convierte en un sistema controlado en lugar de una operación reactiva.
En la industria de dispositivos médicos, este nivel de control no es opcional. Es fundamental.